揭秘铅酸蓄电池:充放电的化学奥秘与方程式
铅酸蓄电池是一种常见的蓄电池类型,广泛应用于各种设备和系统中。为了全面理解铅酸蓄电池的工作原理,深入探讨其充放电方程式显得尤为重要。本文将详细解析铅酸蓄电池的充放电化学反应方程式,帮助读者深入了解这一关键技术。

铅酸蓄电池充放电方程式
铅酸蓄电池的充放电过程是基于铅和铅(IV)氧化物之间的可逆化学反应。在放电过程中,电池对外电路输出电能,而在充电过程中,电池从外部电源获得电能。以下分别详细解析铅酸蓄电池的放电和充电方程式。

放电过程
放电时,铅酸蓄电池的正极和负极分别与硫酸电解液发生反应,生成硫酸铅(PbSO₄)。这一过程的化学反应方程式可以表达如下:

正极反应:
\[PbO_2 + 2e^- + SO_4^{2-} + 4H^+ \rightarrow PbSO_4 + 2H_2O\]
负极反应:
\[Pb - 2e^- + SO_4^{2-} \rightarrow PbSO_4\]
总反应方程式为:
\[PbO_2 + 2H_2SO_4 + Pb \rightarrow 2PbSO_4 + 2H_2O\]
从上述方程式可以看出,放电时正极的活性物质二氧化铅(PbO₂)和负极的活性物质金属铅(Pb)与硫酸电解液反应,生成硫酸铅和水。这一过程也被称为“双硫酸盐化反应”。
在放电过程中,随着反应的进行,硫酸的浓度逐渐降低,电池内部的电解液体积减少,电池两端的电压也逐渐降低。当电池电压下降到一定程度时,铅酸蓄电池被认为已放电完毕。
充电过程
充电时,铅酸蓄电池从外部直流电源获得电能,使得正极和负极上的硫酸铅被分解还原成原来的活性物质,即二氧化铅和金属铅。同时,正极产生氧气,负极产生氢气,这两种气体在电池内部重新结合生成水回到电解液中。充电过程的化学反应方程式可以表达如下:
正极反应(阳极反应):
\[PbSO_4 + 2H_2O - 2e^- \rightarrow PbO_2 + 4H^+ + SO_4^{2-}\]
负极反应(阴极反应):
\[PbSO_4 + 2e^- \rightarrow Pb + SO_4^{2-}\]
总反应方程式为:
\[2PbSO_4 + 2H_2O \rightarrow PbO_2 + 2H_2SO_4 + Pb\]
这一过程是放电过程的逆反应,即在充电电流的作用下,硫酸铅被还原成二氧化铅和金属铅,电解液中的硫酸浓度逐渐增加,电池两端的电压逐渐上升。当正负极板上的硫酸铅都被还原成原来的活性物质时,充电过程结束。
铅酸蓄电池的充电方法
铅酸蓄电池的充电方法有多种,不同的充电方法具有不同的特点和适用场景。以下是几种常见的充电方法:
恒定电流充电法(恒流充电法)
恒定电流充电法是在充电过程中充电电流始终保持不变。该方法简单易行,但存在一些问题,如最大充电电流受到限制,随着充电过程的进行,蓄电池电压逐渐上升,电流却几乎呈直线衰减。
阶段恒流充电法
为了克服恒定电流充电法的不足,阶段恒流充电法应运而生。该方法将充电过程分为不同阶段,每个阶段使用不同的电流进行充电。一般可分为两个阶段或更多阶段进行。例如,第一阶段以较大的电流进行充电,以尽快恢复大部分电量;第二阶段以较小的电流进行充电,以进一步充满电池并减少气泡对极板活性物质的冲刷。阶段恒流充电法所需充电时间短,充电效果好,能有效延长蓄电池使用寿命。
浮充电法
浮充电法通常用于间歇使用的蓄电池或仅在交流电停电时才使用的蓄电池。浮充电法的优点在于能减少蓄电池的析气率,防止过充电,并且当用电设备大电流用电时,蓄电池能瞬时输出大电流,有助于稳定电源系统的电压。然而,浮充电法也存在一些缺点,如个别蓄电池充电不均衡和充不足电,因此需要进行定期的均衡充电。
脉冲充电法
脉冲充电法是一种采用恒定电流和周期恒定的脉冲充电电流对蓄电池进行充电的方法。在两个充电脉冲之间有一个放电脉冲进行去极化,以提高蓄电池的充电接受能力。这种方法能使蓄电池快速充满容量,但如果不增加防止过充电的保护装置,容易造成强烈的过充电,影响蓄电池的使用寿命。
铅酸蓄电池充放电过程中的极化现象
在铅酸蓄电池的充放电过程中,极化现象是一个重要的问题。极化会导致电池内部电压降低,充电和放电效率下降。极化分为欧姆极化、浓差极化和电化学极化三种类型
- 上一篇: LUXE巨幕与IMAX:究竟有何不同?一探究竟!
- 下一篇: 如何获取“美丽的神话吉他谱
-
 铅酸电池与锂电池在电动车中的应用差异资讯攻略12-04
铅酸电池与锂电池在电动车中的应用差异资讯攻略12-04 -
 电池容量(毫安时)是怎么算出来的?资讯攻略01-25
电池容量(毫安时)是怎么算出来的?资讯攻略01-25 -
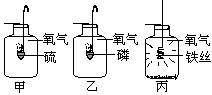 揭秘酸的魔力:五大化学性质及其震撼方程式全解析!资讯攻略10-24
揭秘酸的魔力:五大化学性质及其震撼方程式全解析!资讯攻略10-24 -
 揭秘:酸的五大化学魔法及其神奇反应方程式资讯攻略11-18
揭秘:酸的五大化学魔法及其神奇反应方程式资讯攻略11-18 -
 mAh与Wh之间的神秘换算:轻松掌握电池能量转换!资讯攻略11-03
mAh与Wh之间的神秘换算:轻松掌握电池能量转换!资讯攻略11-03 -
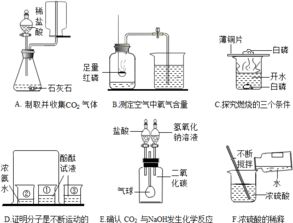 揭秘:红磷燃烧的化学方程式撰写秘籍资讯攻略02-28
揭秘:红磷燃烧的化学方程式撰写秘籍资讯攻略02-28












